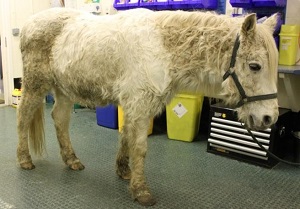
Pony con ipertricosi. Credito di immagine: Edd Knowles
Nonostante il suo nome comunemente usato della malattia equina di Cushing, gli aspetti più interessanti della disfunzione intermedia della pars ipofisaria equina (PPID) sono, infatti, le sue dissomiglianze dalla sindrome di Cushing, in esseri umani o cani., Come suggerisce il nome raccomandato PPID, questa è una malattia che colpisce la pars intermedia della ghiandola pituitaria, non la pars distalis o la ghiandola surrenale. Ciò ha ripercussioni sui modi migliori di diagnosticare e curare la malattia.
FISIOPATOLOGIA SOTTOSTANTE
Molti aspetti della fisiopatologia di questo disturbo sono ancora sconosciuti. Tuttavia, le basi sono relativamente indiscusse. È una malattia neurodegenerativa che colpisce i neuroni dopaminergici periventricolari dell’ipotalamo.,1,2 La perdita di dopamina nel lobo intermedio della ghiandola pituitaria previene gli effetti inibitori della stimolazione del recettore dopaminergico D2 nelle membrane cellulari dei melanotrofi.
In salute, questa inibizione si traduce in una diminuzione della sintesi e del rilascio di peptidi derivati da pars intermedia pro-opiomelanocortina (POMC) e una diminuzione della proliferazione di melanotroph., La perdita di inibizione mediata dalla dopamina provoca inizialmente ipertrofia e iperplasia del lobo intermedio, con un aumento dell’ormone stimolante α-melanociti circolante (α-MSH), adrenocorticotrofina (ACTH), β-endorfina e peptide intermedio simile alla corticotropina (CLIP).3 Con la progressione della malattia, la pars intermedia si allarga ulteriormente, formando un adenoma che può comprimere le strutture pituitarie, ipotalamiche e cerebrali adiacenti.4
La causa della degenerazione dei nervi contenenti dopamina è ancora sconosciuta., Vi è evidenza di accumulo di marcatori di stress ossidativo,2 proteine terminali nervose misfolded2 e possibilmente alterata clearance proteica,5 ma se queste sono cause o conseguenze della malattia non è ancora stato dimostrato.
DIFFICOLTÀ DI DIAGNOSI
La diagnosi di PPID può essere impegnativa e controversa. Come per molte malattie progressive, l’identificazione dei casi avanzati è semplice, ma quella dei primi casi è più difficile.,
‘Gli aspetti più interessanti del PPID equino sono, infatti, le sue differenze dalla sindrome di Cushing’
Un’ulteriore complicazione specifica per gli equidi è legata al loro adattamento alla sopravvivenza in climi temperati. I cavalli, e in particolare i pony, hanno la capacità di regolare il loro metabolismo per immagazzinare energia quando i nutrienti sono prontamente disponibili in primavera e in estate, in preparazione per l’autunno e l’inverno quando i nutrienti sono scarsi., I cambiamenti di temperatura stagionali provocano la crescita di un pelo lungo in inverno che viene versato in primavera. La pars intermedia è coinvolta in questi cambiamenti stagionali, come dimostra la variazione stagionale delle concentrazioni di ACTH e MSH, la risposta del cortisolo 6 alla soppressione del desametasone7 e la risposta dell’ACTH alla stimolazione dell’ormone di rilascio della tireotropina (TRH).,8,9
Gli studi che studiano i metodi diagnostici sono spesso ostacolati dalla mancanza di un test ante-mortem “gold standard”, e quegli studi che utilizzano la diagnosi post-mortem possono anche essere imperfetti a causa della variazione stagionale dell’aspetto istologico della pars intermedia10 e delle incongruenze nelle diagnosi istologiche tra patologi.11 Sono stati compiuti recenti progressi nella diagnosi post mortem; 12 l’utilizzo di questi metodi può consentire ulteriori indagini sui test ante mortem., L’unico test che non determina falsi positivi è la presenza di ipertricosi, un segno clinico patognomonico presente negli stadi più avanzati della malattia.
Le attuali raccomandazioni per la diagnosi si basano su un algoritmo progettato dal gruppo di Endocrinologia equina.13 Negli animali che mostrano evidenti segni clinici di PPID, l’ACTH a riposo è il test di prima linea. Se questo è alto, rispetto al range di riferimento destagionalizzato,14,15, allora il trattamento deve essere avviato., Se l’ACTH a riposo è normale e negli animali con segni sottili di PPID, il test di stimolazione TRH deve essere eseguito e l’ACTH misurato.16 Una risposta esagerata è visto in individui affetti da PPID.
La laminite è stata a lungo collegata al PPID. La teoria attuale è che l’iperinsulinemia è il principale fattore di rischio per la laminite e PPID può essere un fattore di rischio per l’iperinsulinemia. L ‘ attuale test raccomandato per il rischio di iperinsulinemia clinicamente significativa è la misurazione della risposta insulinica allo zucchero orale., Se si osserva una risposta esagerata, è necessaria una gestione per ridurre l’accesso al pascolo e alti livelli di mangime a base di carboidrati non strutturali.
APPROCCI AL TRATTAMENTO
il Trattamento è variato negli anni, ma, dal momento che l’autorizzazione di pergolide mesilato per l’uso in PPID in cavalli nel 2011 (Prascend®; Boehringer Ingelheim Vetmedica), le alternative di cyproheptadine (un antagonista della serotonina) e trilostane (un inibitore della steroidogenesi surrenalica) sono raramente utilizzati.,
Pergolide è un agonista del recettore della dopamina, che agisce per ripristinare l’inibizione mediata dal recettore della dopamina dei melanotrofi della pars intermedia. Il trattamento con pergolide riduce le concentrazioni basali di ACTH17 e migliora i segni clinici nella maggior parte dei casi, con l’effetto indesiderato più comune che è l’inappetenza.18,19 Se pergolide non determina un miglioramento sufficiente, si può effettuare un trattamento con ciproeptadina.
MIGLIORARE LA PROGNOSI
Mentre il trattamento può migliorare i segni clinici e la qualità della vita dei cavalli con PPID, la condizione può solo essere gestita e non curata., La malattia colpisce animali di mezza età a più anziani, con vari gradi dei seguenti segni clinici: ipertricosi, sudorazione anormale, predisposizione alla laminite e/o infezioni, perdita di massa muscolare, letargia, poliuria e polidipsia.20 La combinazione di una gestione farmacologica efficace e di supporto può anecdotally portare a una migliore qualità della vita per diversi anni, anche se gli studi randomizzati controllati sono carenti in questo settore.,
Il PPID equino ha poche somiglianze con la sindrome di Cushing umana o canina; riconoscere le differenze tra le condizioni ha facilitato i progressi nelle aree impegnative di comprensione della fisiopatologia del PPID equino e del modo migliore per diagnosticarlo.
Elizabeth Finding
Anatomy Demonstrator, Royal Veterinary College, London
- McFarlane D 2007 Ageing Research Reviews 6 54-63.
- McFarlane D et al. 2005 Journal of Neuroendocrinology 17 73-80.
- Orth DN et al. 1982 Endocrinologia 110 1430-1441.
- Boujon CE et al., 1993 Journal of Comparative Pathology 109 163-178.
- McFarlane D et al. 2011 Journal of Veterinary Internal Medicine 25 750 Abst 85B.
- Beech J et al. 2009 Journal of American Veterinary Medical Association 235 715-722.
- Donaldson MT et al. 2005 Journal of Veterinary Internal Medicine 19 217-222.
- Diez de Castro E et al. 2014 Endocrinologia animale domestico 48 77-83.
- Fredrick J et al. 2014 Journal of Veterinary Internal Medicine 28 1104 Abst E-8.
- Cordero M et al. 2012 Journal of Equine Veterinary Science 32 75-79.
- McFarlane D et al., 2005 American Journal of Veterinary Research 66 2055-2059.
- Leitenbacher J& Herbach N 2016 Journal of Comparative Pathology 154 215-224.
- Frank N et al. 2015 Raccomandazioni per la diagnosi e il trattamento di PPID
- Copas VEN & Durham AE 2012 Equine Veterinary Journal 44 440-443.
- McGowan TW et al. 2013 Rivista veterinaria equina 45 66-73.
- Beech J et al. 2011 Journal of American Veterinary Medical Association 238 1305-1315.
- McFarlane D et al., 2016 Journal of Veterinary Pharmacology and Therapeutics doi: 10.1111 / jvp.12339.
- Donaldson MT et al. 2002 Journal of Veterinary Internal Medicine 16 742-746.
- Perkins GA et al. 2002 Equine Veterinary Journal 34 679-685.
- McFarlane D 2011 Cliniche veterinarie del Nord America: Pratica equina 27 93-113.

Lascia un commento