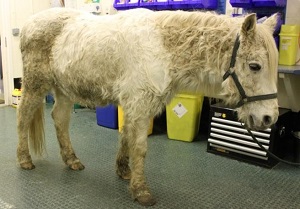
Ponei cu hipertricoză. Imagine de credit: Edd Knowles
În ciuda numelui său frecvent utilizat de boala Cushing ecvină, cele mai interesante aspecte ale hipofizei ecvine pars intermedia disfunctie (PPID) sunt, de fapt, diferențele sale de sindromul Cushing, fie la oameni sau câini., După cum sugerează denumirea recomandată PPID, aceasta este o boală care afectează intermedia pars a glandei pituitare, nu pars distalis sau glanda suprarenală. Acest lucru are repercusiuni pentru cele mai bune metode de diagnosticare și tratare a bolii.multe aspecte ale fiziopatologiei acestei tulburări sunt încă necunoscute. Cu toate acestea, elementele de bază sunt relativ incontestabile. Este o boală neurodegenerativă care afectează neuronii dopaminergici periventriculari ai hipotalamusului.,1,2 pierderea dopaminei în lobul intermediar al glandei pituitare previne efectele inhibitoare ale stimulării receptorului dopaminergic D2 în membranele celulare ale melanotrofelor.
În domeniul sănătății, această inhibare a rezultat într-o scădere în sinteza și eliberarea de pars intermedia pro-opiomelanocortin (a AJUTA)-derivate peptide și o scădere în melanotroph proliferare., Pierderea de dopamină mediate prin inhibarea inițial rezultate în hipertrofia și hiperplazia de lobul intermediar, cu o creștere în circulant α-melanocite-hormon de stimulare (α-MSH), adrenocorticotrophin (ACTH), β-endorfina și corticotrofinei-ca intermediar peptide (CLIP).3 cu progresia bolii, pars intermedia se mărește în continuare, formând un adenom care poate comprima structurile hipofizare, hipotalamice și cerebrale adiacente.4
cauza degenerării nervilor care conțin dopamină este încă necunoscută., Există dovezi de acumulare de markeri ai stresului oxidativ, 2 proteine terminale nervoase rătăcite2 și,eventual, clearance-ul proteic modificat, 5 dar dacă acestea sunt cauze sau consecințe ale bolii este încă nedovedită.
dificultăți de diagnosticare
diagnosticul PPID poate fi provocator și controversat. Ca și în cazul multor boli progresive, identificarea cazurilor avansate este simplă, dar cea a cazurilor timpurii este mai dificilă.,
‘Cele mai interesante aspecte ale ecvină PPID sunt, în fapt, deosebirile de sindromul Cushing’
O complicație suplimentară specific al ecvinelor este legată de adaptarea lor la supraviețuire în zonele cu climă temperată. Caii, și în special poneii, au capacitatea de a-și regla metabolismul pentru a stoca energie atunci când nutrienții sunt ușor disponibili primăvara și vara, în pregătirea toamnei și a iernii, când nutrienții sunt puțini., Schimbările de temperatură sezoniere au ca rezultat creșterea unui strat de păr lung în timpul iernii, care este vărsat în primăvară. Pars intermedia este implicat în aceste schimbările sezoniere, cum este demonstrat de variație sezonieră în ACTH și MSH concentrații,6 cortizol ca răspuns la dexametazonă suppression7 și ACTH răspuns la thyrotrophin-releasing hormone (TRH) de stimulare.,8,9
Studii care investighează metode de diagnostic sunt de multe ori împiedicată de lipsa de o „standardul de aur” ante-mortem de testare, și aceste studii folosind post-mortem diagnosticul poate fi, de asemenea, eronată datorită variației sezoniere aspectul histologic al pars intermedia10 și neconcordanțe în histologice diagnostice între patologi.11 progrese recente în diagnosticul post-mortem au fost făcute;12 utilizarea acestor metode poate permite investigarea ulterioară a testelor ante-mortem., Singurul test care nu are rezultate fals pozitive este prezența hipertricozei, un semn clinic patognomonic prezent în stadiile mai avansate ale bolii.recomandările actuale pentru diagnostic se bazează pe un algoritm conceput de grupul de Endocrinologie ecvină.13 la animalele care prezintă semne clinice evidente de PPID, ACTH în repaus este testul de primă linie. Dacă acest lucru este ridicat, în comparație cu intervalul de referință ajustat sezonier,14,15, atunci trebuie inițiat tratamentul., Dacă ACTH în repaus este normal și la animalele cu semne subtile de PPID, trebuie efectuat testul de stimulare TRH și măsurat ACTH.16 la persoanele afectate de IDP se observă un răspuns exagerat.Laminita a fost mult timp legată de PPID. Teoria actuală este că hiperinsulinemia este principalul factor de risc pentru laminită, iar PPID poate fi un factor de risc pentru hiperinsulinemie. Testul actual recomandat pentru riscul de hiperinsulinemie semnificativă clinic este măsurarea răspunsului insulinei la zahărul oral., Dacă se observă un răspuns exagerat, este necesară o gestionare pentru a reduce accesul la pășune și niveluri ridicate de hrană cu carbohidrați nestructurali.
ABORDĂRI PENTRU TRATAMENTUL
Tratament a variat de-a lungul anilor, dar, întrucât autorizarea de pergolid mesilat pentru utilizarea în PPID în cai în 2011 (Prascend®; Boehringer Ingelheim Vetmedica), alternativele de ciproheptadină (un antagonist serotonină) și trilostane (un inhibitor al steroidogenezei adrenale) sunt rar folosite.,Pergolida este un agonist al receptorilor dopaminergici, care acționează pentru a restabili inhibarea mediată de receptorii dopaminergici a melanotrofelor pars intermedia. Tratamentul cu pergolidă reduce concentrațiile bazale de ACTH17 și îmbunătățește semnele clinice în majoritatea cazurilor, cel mai frecvent efect secundar fiind inapetența.18,19 dacă pergolida nu are ca rezultat o ameliorare suficientă, tratamentul cu ciproheptadină poate fi testat.în timp ce tratamentul poate îmbunătăți semnele clinice și calitatea vieții cailor cu BIPP, afecțiunea poate fi gestionată și nu vindecată., Boala afectează animalele de vârstă mijlocie la animalele mai în vârstă, cu grade diferite de următoarele semne clinice: hipertricoză, transpirație anormală, predispoziție la laminită și/sau infecții, pierderea masei musculare, letargie, poliurie și polidipsie.20 combinația dintre un tratament farmacologic eficace și un tratament de susținere poate duce anecdotic la îmbunătățirea calității vieții timp de mai mulți ani, deși lipsesc studii controlate randomizate în acest domeniu.,
Ecvină PPID are puține asemănări umane sau canin sindromul Cushing; recunoscând diferențele dintre condiții a facilitat progresul în provocatoare domenii de înțelegerea fiziopatologiei ecvină PPID și cum cel mai bine pentru a diagnostica.pentru mai multe informații, consultați Notificarea cu privire la cookie-uri

Lasă un răspuns